Einführung
Für die verschiedenen Amputationshöhen sind spezielle Aspekte zu beachten. Die Entfernung von Sehnenansätzen kann zu einer Änderung des muskulären Gleichgewichts führen (z.B. Chopart-Amputationen) wobei sich über die letzten Jahrzehnte verschiedene Pinzipien herauskristallisiert haben, bei deren Beachtung in den meisten Fällen trotz Amputation ein gutes funktionelles Ergebnis erzielt werden kann. Trotz einzelner auch sportlicher Höchstleistungen sind Patienten nach Amputationen eingeschränkt und zwar umso mehr, je weiter körperwärts amputiert worden ist. In Einzelfällen kann aber auch umgekehrt ein kontrakter, schmerzhafter und steifer Fuß funktionell für den Patienten ungünstiger und mit mehr Einschränkungen verbunden sein als eine gute Prothese. Meist handelt es sich hier um Patienten nach schweren Quetschverletzungen mit ausgedehnten Nervenschäden und Muskelkontrakturen. Auch wenn heute Amputationen in der überwiegenden Zahl bei der Diagnose eines Diabetes mellitus erfolgen, gelten die im folgenden dargestellten Prinzipien in der Mehrzahl auch bei Amputationen auf der Basis anderer Indikationen.
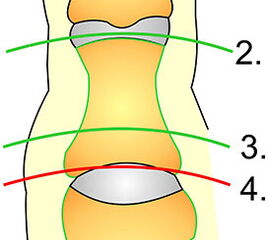
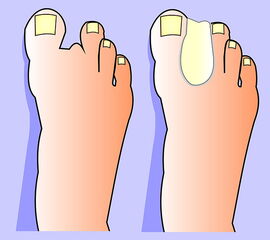
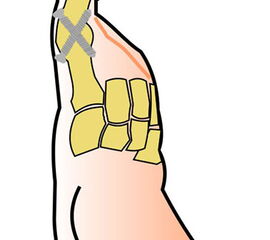
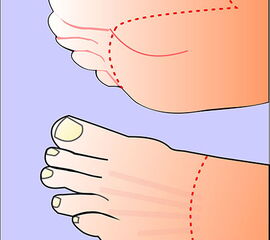
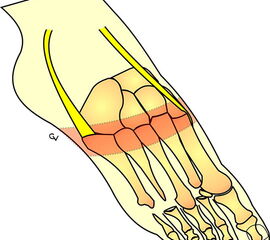
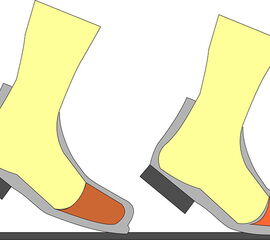
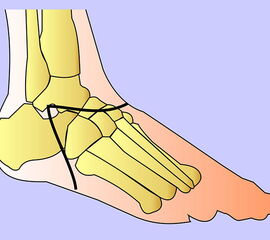
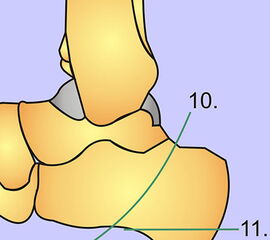
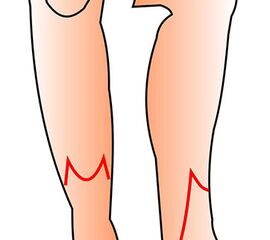
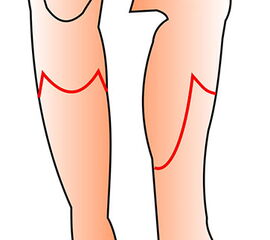
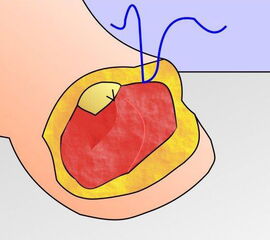
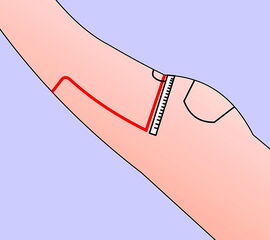
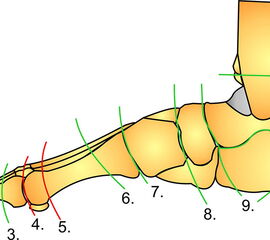
Die Amputationslinien am Fuß, die sich uns bewährt haben, sind in der Abb. 1 schematisch dargestellt.
Amputationen am ersten Strahl
Amputationen innerhalb der Großzehe
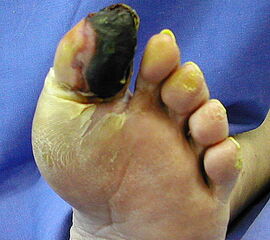
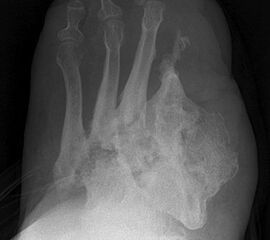
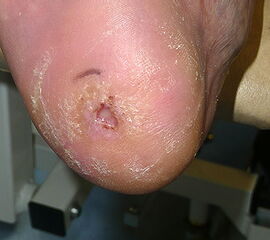
Indikationen:
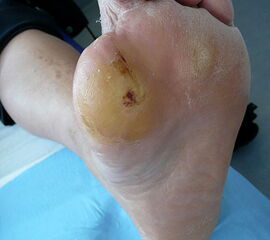
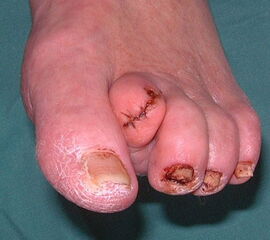
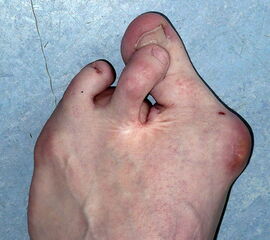
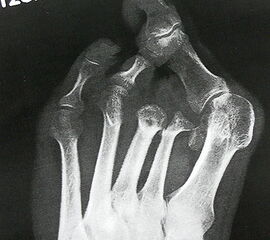
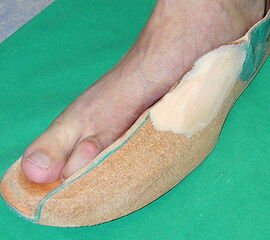
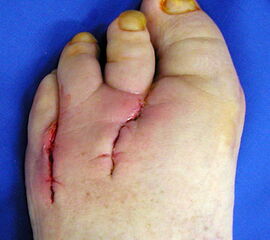
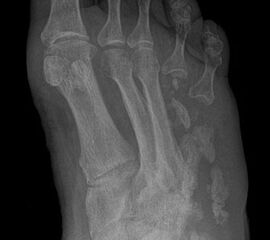
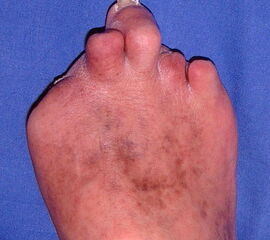
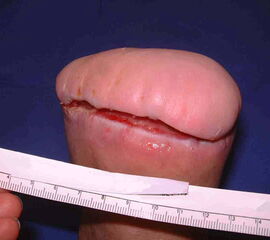
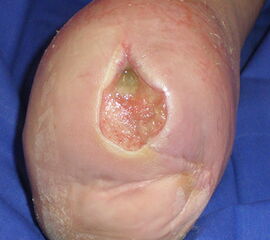
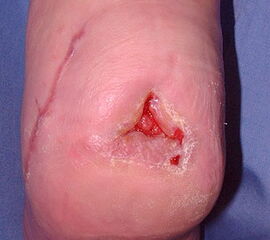
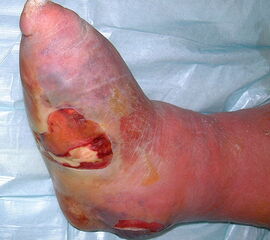
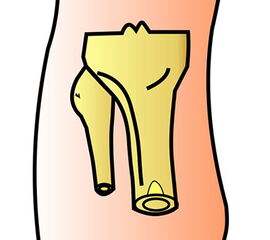
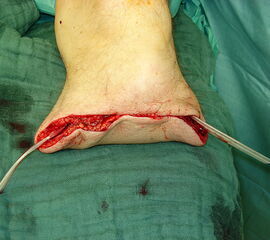
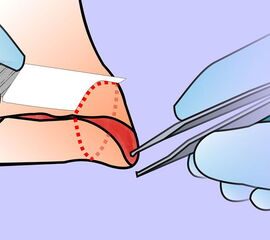
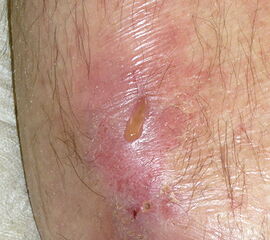
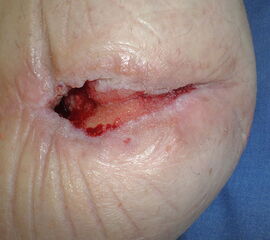
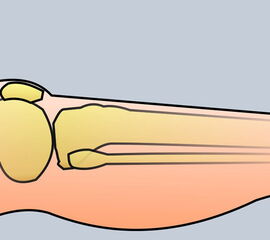
Nekrose an der Großzehe (Abb. 2)
nicht revaskularisierbare Ischämie,
neuropathisches Druckulkus mit Infektion,
(schwere Nagelveränderungen, selten)
Alternativen
Es muss ausgeschlossen sein, dass durch Zehen erhaltende Maßnahmen wie Revaskularisation oder Stellungskorrektur (Tenotomie, Arthrodese, Resektion) eine Heilung zu erzielen ist.
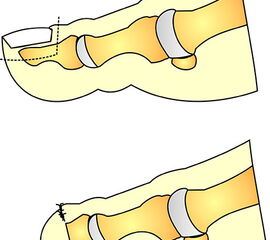
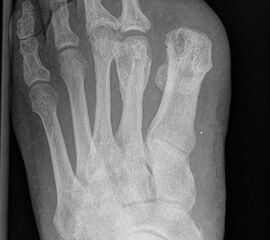
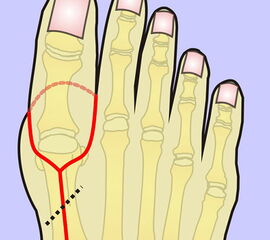
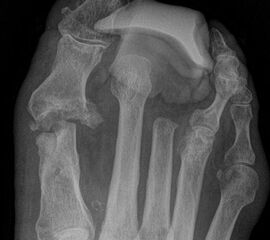
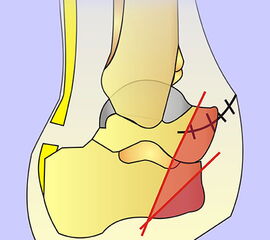
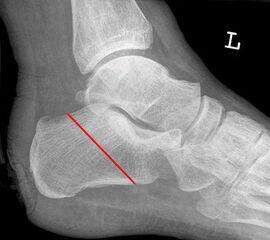
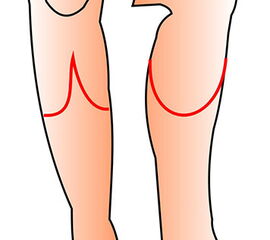
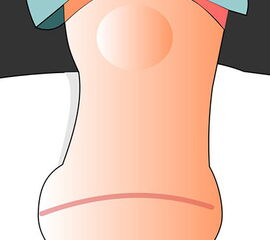
Die bewährten Amputationslinien am 1. Strahl finden sich in Abb. 3.
Technik:
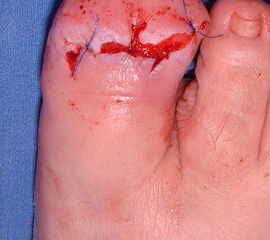
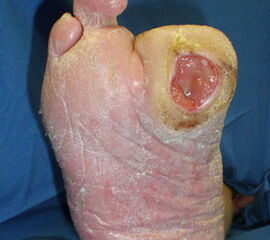
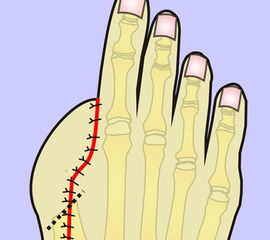
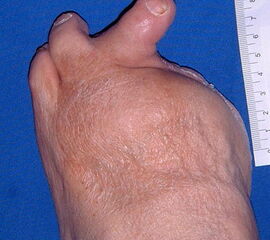
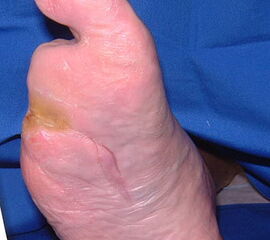
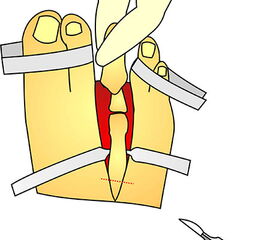
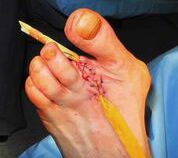
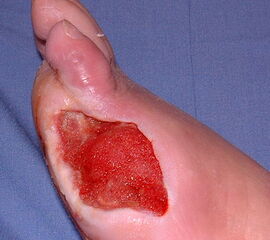
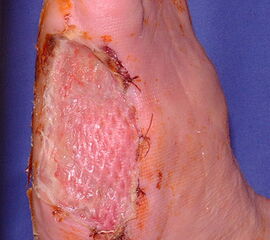
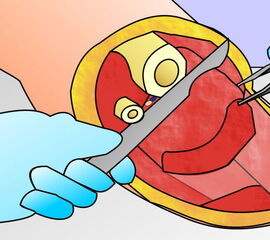
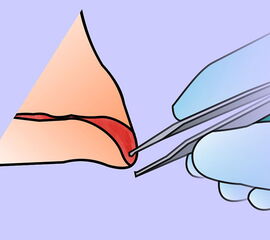
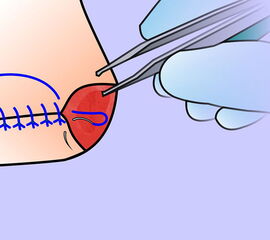
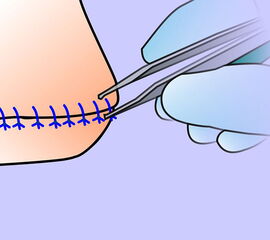
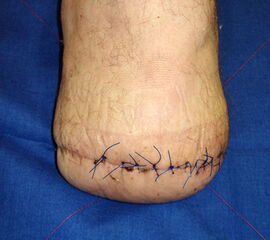
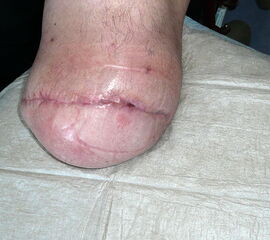
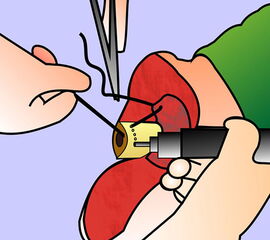
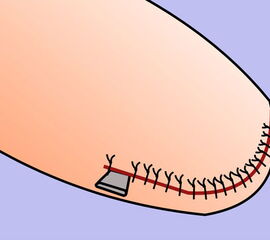
Exzision des Endglieds unter Bildung eines plantaren Lappens (Abb. 4). Die Absetzung kann im Endglied, im Endgelenk als Exartikulation oder im Grundglied distal der Ansätze der kurzen Beuger vorgenommen werden. Der Verschluss der Wunde durch Nähte ist wegen des längeren plantaren Lappens meist nur „mokassinartig“ möglich. Die Unregelmäßigkeiten werden im Verlauf der Wundheilung spontan ausgeglichen (Abb. 5).
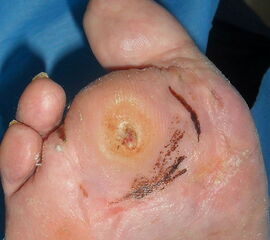
Beachten:
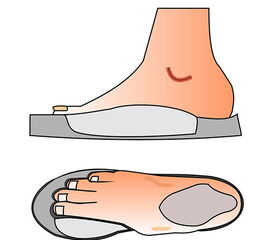
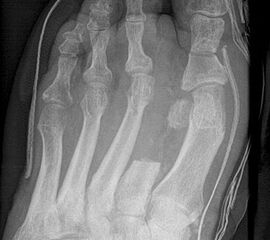
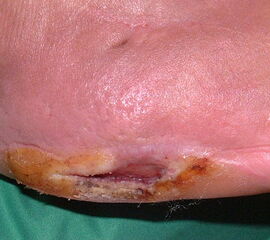
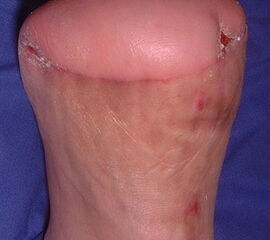
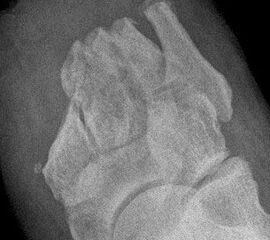
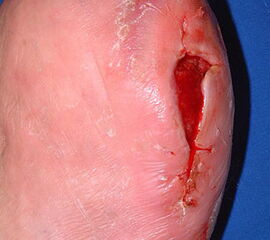
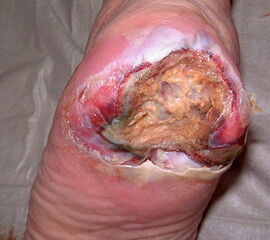
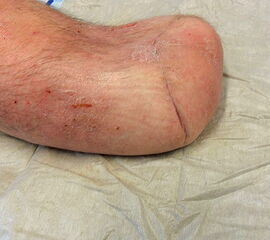
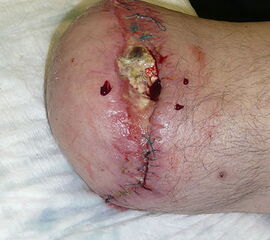
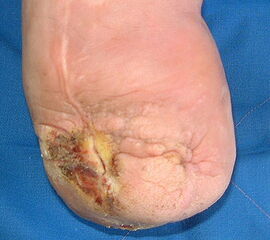
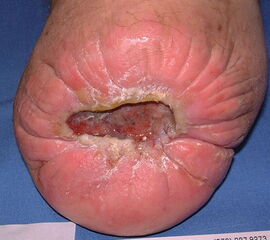
Exartikulationen im Großzehengrundgelenk bedingen bei Neuropathie häufig Druckulzerationen am Metatarsalekopf (Abb. 6, 7). Wenn vertretbar, wird die Basis des Grundglieds mit den Sehnensansätzen erhalten, um chronische Druckprobleme zu vermeiden (Abb. 8). Im Falle einer Exartikulation ist dem Druck unter dem Metatarsale-I-Kopf große Aufmerksamkeit zu widmen. Durch eine Entfernung der Sesambeine und Abtragen von plantaren knöchernen Prominenzen kann die Auflagefläche vergrößert und damit der Druck reduziert werden. Postoperativ muss der Mittelfuß durch Einlagen in seinem Gewölbe breitflächig abgestützt werden (Abb. 9). Ansonsten resultiert ein Plattfuß mit Pronation und Abduktion.
Amputation im 1. Mittelfußknochen
Alternative:
Bei eitrigen Osteoartritiden des Grundgelenks reicht häufig die Resektion der Gelenkanteile. Die Wunde wird offen gelassen und heilt per secundam.
Operationstechnik:
Wir bevorzugen die Amputation im Mittelfußknochen gegenüber der Exartikulation im MTP Gelenk (Abb. 10): Ein Ulkus an dem Metatarsale I Stumpf ist durch stützende Einlage zu verhindern.
Tennisschlägerartige Umschneidung der Großzehe (Abb. 11). Das Metatarsale wird so osteotomiert, dass an der Medial- und Plantarseite keine Knochenkanten verbleiben (Abb. 12).
Wird das Metatarsale I im Schaftbereich abgesetzt, muss der Fuß analog zur Amputation im Grundglied zur Verhinderung eines Plattfußes bzw. eines Druckulkus am Stumpfende medial langstreckig gut abgestützt werden (Abb. 9). Die Einlegesohle muss einen integrierten Platzhalter aufweisen, um die Varuskippung der 2. Zehe zu verhindern.
Amputationen an den Kleinzehenstrahlen
Amputation innerhalb der Kleinzehe
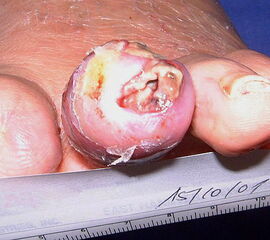
Indikationen:
Chronisches Ulkus mit Infektion (Abb. 13).
Ein Ulkus ohne Infektion ist keine Indikation zur Amputation. Wenn die Zehe eine Überlänge aufweist und aus diesem Grunde erneute Ulzerationen zu erwarten sind, kommt neben der Resektion des PIP-Gelenks die Endgliedamputation in Betracht.
Alternativen:
Bei nichtinfiziertem Zehenspitzenulkus aufgrund einer Krallenzehbildung ist das bevorzugte Vorgehen die perkutane Durchtrennung der langen Beugesehne 1. Daneben kann eine Stellungskorrektur - z.B. eine klassische Hohmann Resektionsarthroplastik - eine Heilung des Ulkus herbeiführen.
Auch bei infizierten Ulzerationen im Bereich des proximalen Interphalanagealgelenkes (PIP)
kann eine Resektion des Gelenkes sinnvoll sein. Dadurch wird eine Verkürzung der Zehe
und ein Ausgleich der Krallenstellung erreicht.
Amputationshöhen:
Bei einschmelzender Infektion kann die Zehe auf jedem Niveau abgesetzt werden.
Wegen des Risikos einer Ulzeration am Metatarsalekopf (Abb. 14) sollte die Exartikulation im Grundgelenk vermieden werden. Günstiger ist es, falls möglich, einen kurzen Grundgliedstumpf als Platzhalter zu belassen (Abb. 15). Wenn Zehen in eine Lücke zu kippen drohen, kann die mit einem Platzhalter verhindert werden (Abb. 16, 17)
Technik:
Die Zehe wird unter Bildung eines größeren plantaren Lappens fischmaul-artig umschnitten. Anschließend wird der Knochen soweit gekürzt, dass ein spannungsfreier Hautverschluss möglich ist.
Cave:
Es ist ungünstig, wenn wenige Kleinzehen lateral belassen werden. Das führt zum Kippen der Nachbarzehen oder zur Fehlstellung der verbliebenen Zehen (Abb. 18 - 20) und schließt eine optimale schuhtechnische Versorgung aus. Weitere Druckulzera sind zu erwarten. Die Großzehe kann als einzige Zehe belassen werden, wobei dann bisweilen die Arthrodese im Großzehengrundgelenk zur Stabilisierung ratsam ist (Abb. 21, 22).
Nachbehandlung:
Verbandschuh bis zur Wundheilung (Vorfußentlastungsschuhe sind für Neuropathiker zu instabil). Wenn bei den verbliebenen Zehen eine Neigung zur Kippung in die entstandene Lücke besteht, muss ein Platzhalter oder eine Orthose angepasst werden, um die Gradstellung der Zehen zu gewährleisten. Ein Platzhalter wird meist in eine Einlage integriert. Technisch läßt sich dies besonders gut am lateralen oder medialen Fußrand umsetzen (Abb. 23).
Amputation der Kleinzehen im Mittelfußknochen
Die Strahlresektion sollte wegen der Gefahr eines Ulkusrezidivs der Exartikulation im MTP Gelenk vorgezogen werden!
Alternativen:
Resektion eines oder mehrerer Mittelfußköpfe unter Belassen der Zehen
Technik
Die Zehe wird tennisschlägerartig umschnitten (Abb. 24). Falls ein infiziertes plantares Ulkus vorliegt, kann die Exzision dieses mit einbeziehen. Dies ist jedoch meistens nicht erforderlich. Das proximale Inzisionsende reicht bis an das TMT Gelenk. Das Metatarsale wird möglichst proximal osteotomiert, wobei am 1. Strahl eine Kantenbildung nach medial und 5. Strahl eine nach lateral vermieden werden muss. Es soll erreicht werden, dass die Nachbarzehen sich annähern, um das Kippen einzelner Zehen zu vermeiden (Abb. 25). Es wurde vorgeschlagen, die Fußverschmälerung durch einen Minifixateur, der zwischen 1. und 5. Mittelfußknochen angelegt wird, zu begünstigen (Bevilaqua 2013). In unserem Patientengut hat sich hierfür nie die Notwendigkeit ergeben, da sich die Mittelfußköpfe durch Narbenzug spontan annäherten und narbig stabil verheilten (Abb. 26). Bereits nach wenigen Wochen hat sich der Fuß verschmälert und bietet ein kosmetisch günstiges Ergebnis (Abb. 27).
Cave:
Die Knochenenden müssen so gestaltet werden, dass sie keinen Druck auf die Haut ausüben können. Wenn sich die Wundränder nicht durch Nähte verschließen lassen (z.B. nach Infektion), wird in den nicht belasteten Regionen eine Spalthautdeckung vorgenommen (Abb. 28, 29), wenn eine infektfreie Granulation vorliegt.
Wird der Ansatz des M. fibularis (peroneus) brevis bei Amputation des 5. Strahls entfernt, kommt es durch das muskuläre Ungleichgewicht zu einer Supination mit Vorfußadduktion und nachfolgend zu einer vermehrten Druckbelastung am Außenrand des Fußes (Abb. 30, 31). Um einer chronischen Ulzeration vorzubeugen, muss die Fehlstellung beseitigt werden, meist durch Transfer der Tibialis anterior Sehne.
Transmetatarsale Amputation (TMA)
Die TMA ist technisch relativ einfach durchzuführen. Die Verringerung der Stand- und Lauffläche ist mit einer Sohlenversteifung weitgehend auszugleichen, sodass die Patienten meist sehr zufrieden sind. Sie ist funktionell einer Amputation unter Belassen von ungünstig stehenden Zehen eindeutig vorzuziehen.
Indikationen:
- Nicht revaskularisierbare Ischämie
- ausgedehnte eitrig-entzündliche Schäden an mehreren Zehen,
- belassene störende Kleinzehen (Abb. 32).
Technik:
Bildung eines großen plantaren Lappens, der bis zu den Basen der Zehen reicht (Abb. 33). Die Knochen werden im Bereich der proximalen Drittelpunkte durchtrennt (Abb. 34), wobei darauf zu achten ist, dass die Enden der Metatarsalia ein harmonisches abgerundetes Profil ergeben (Abb. 35), um Druckspitzen unter der Haut zu vermeiden. Der Metatarsale-III-Stumpf ist also am längsten, der vom Metatarsale I und V sind am kürzesten. Es erfolgt eine Abschrägung aller Metatarsalia nach plantar sowie des Metatarsale I nach medial und des Metatarsale V nach lateral. Die Sehnen der Zehenbeuger und -strecker werden etwas gekürzt. Die Gefäße werden koaguliert. Die Nerven sind im schwieligen Gewebe oft nur schwer darzustellen. Sie werden koaguliert und gekürzt, sollten sie intraoperativ identifizierbar sein. Schmerzhafte Neurome sind bei Patienten mit Neuropathie nicht zu befürchten.
Um das Risiko der Ausbildung eines Stumpfulkus zu verringern, wird von verschiedenen Autoren empfohlen, vor der eigentlichen Amputation den Zug des M. Trizeps surae zu reduzieren. Es gibt verschiedene Techniken, wobei uns das Faszienrelease am proximalen, medialen Gastrocnemiuskopf am günstigsten erscheint 2.
Werden die Sehnenansätze des M. tibialis anterior und/oder M. fibularis (peroneus) brevis entfernt, kann die Sehne des M. extensor hallucis longus bzw. des M. extensor digitorum longus auf einen medialen bzw. lateralen Mittelfußknochen transponiert werden (Bevilaqua 2013). Alternativ ist die Insertion der Sehne des M. fibularis brevis in das Cuboid mit Tenodese zur Sehne des M. fibularis longus möglich.
Wundverschluss
Der Wundverschluss erfolgt nach Einlegen eine Drainage durch lockere Subkutan- und Hautnähte. Bei schweren Infektionen bleibt die Wunde offen. Es empfiehlt sich ein Verband mit mäßiger Kompression, um Sickerblutungen zu stillen. Sobald eine infektfreie Granulation des Wundgrundes eingetreten ist, erfolgt der finale Wundverschluss. Dabei ist darauf zu achten, keine Hohlräume in der Tiefe zu belassen. Geringe Wunddehiszenzen verschließen sich spontan (Abb. 36, 37).
Fehler:
Den plantaren Lappen sollte man nicht zu klein zu präparieren. Dies erschwert den Wundverschluss oder macht ihn unmöglich.
Wird der Ansatz der Sehne des M. fibularis brevis bei erhaltenem Tibialis anterior entfernt, resultieren aufgrund des muskulären Ungleichgewichts eine Adduktion und eine Supination. Dies führt zur Ulzerationen am Fußaußenrand. Wenn der Ansatz der Sehne des M. tibialis anterior (bei Erhalt der Fibularis brevis) entfernt wird, resultiert eine Abduktion, Pronation und Equinus-Stellung. Sollte die Entfernung der Sehnenansätze unvermeidbar sein, müssen Lösungen zum Ersatz gefunden werden: z.B. durch Sehnentransposition oder korrigierende Arthrodesen.
Wenn die Metatarsalia nicht bogenförmig, sondern gerade osteotomiert werden, drohen Druckulzera (Abb. 38, 39).
Ein korrekt gestalteter TMA Stumpf lässt sich schuhtechnisch gut versorgen.
Nachbehandlung
Patienten mit TMA werden mit einem Schuh versorgt, der eine Sohlenversteifung und einen Platzhalter für die fehlenden distalen Fußanteile aufweist (Abb. 40). Dadurch werden Druckspitzen am den MT-Stümpfen verhindert, die zur Ulzeration führen können.
Amputation in der Lisfranc-Linie
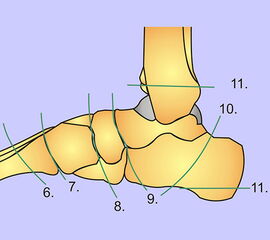
Auf dem Niveau der Tarso-metatarsal-Gelenke (TMTG) kommen die operationstechnischen Prinzipien der TMA analog zur Anwendung (Abb. 41). Nach Absetzen in der Gelenkreihe werden die Knochenkanten nach medial, plantar und lateral abgeschrägt. Wesentlich ist, dass bei einer Amputation in der Lisfranc-Gelenklinie die Sehnenansätze des M. fibularis (peroneus) brevis immer und die Sehne des M. tibialis anterior häufig entfernt. Um eine Spitzfußstellung bzw. störende Seitdeviation zu umgehen, sollte nach Möglichkeit eine Resinsertion vorgenommen werden. Alternativen sind eine Durchtrennung der Achilles- und Tibialis-posterior-Sehne mit einer Sehnentransposition.
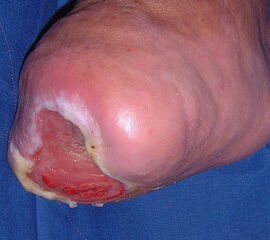
Cave!
Wird der Fußheber desinseriert, kommt es häufig zu einem Spitzfuß mit Stumpfulkus (Abb. 42). Die Prophylaxe und Behandlung bestehen in der Achillessehnendurchtrennung (entspr. Abb. 50). Eine Refixation der Fußhebersehne ist bei vorhandenem Stumpfulkus infektionsgefährdet und nicht erfolgversprechend. Besteht ein Spitzfuß über viele Monate, ist dieser regelmäßig durch eine Arthrofibrose fixiert. Dann müssen alle am Unterschenkel dorsal verlaufenden Sehnen durchtrennt, das Gelenk offen arthrolysiert und die 0-Grad-Stellung temporär mit einem K-Draht fixiert werden. Alternativ ist eine Arthrodese im oberen evtl. auch unteren Sprunggelenk möglich.
Nachbehandlung
Die schuhtechnische Versorgung erfolgt durch eine Sohlenversteifung und Platzhalter für die fehlenden distalen Fußanteile wie bei einer TMA (Abb. 40).
Amputation in der Chopartlinie
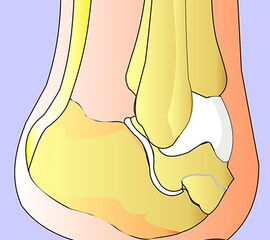
Bei der Chopartamputation – (wie auch bei der Amputation in der Bona-Jäger-Linie) – ist zu beachten, dass die Ansätze der Fuß- und Zehenheber entfernt werden, also der Rückfuß durch den Zug des M. triceps surae eine Equinusstellung einnimmt (Abb. 43). Die Folge können hartnäckige Ulzerationen an der Spitze des Stumpfes sein (Abb. 44). Neben der Durchtrennung der Achillessehe (Abb. 45) sollte die plantare, distale Knochenkante abgerundet werden (Abb. 46).
Um das Stumpfulkus zu vermeiden, muss die Achillessehne im Rahmen der Amputation durchtrennt werden; besser noch ist eine Resektion eines Segmentes der Sehne, damit ein erneutes Zusammenwachsen sicher auszuschließen ist. Das Sprunggelenk stabilisiert sich durch Fibrosierung. Eine Fixation der Streckersehnen an Talus und Calcaneus, wie in der Literatur beschrieben, führen wir nicht durch, weil die Kraftentwicklung bei dem kurzen Hebelarm sehr schwach ist (Brodsky 2007).
Alternative:
Bei eitriger Osteomyelitis der distalen Tarsalknochen reicht es bisweilen, alle Knochen zwischen Talus-Calcaneus und den Basen der Metatarsalia einschließlich des Taluskopfes zu entfernen. Es resultiert ein normal aussehender Fuß, der sich gut schuhtechnisch versorgen lässt (Baumgartner 1995).
Technik:
Das operative Vorgehen entspricht bezüglich der Inzision dem bei der Lisfrancamputation etwas nach proximal versetzt. Die Achillessehne wird über eine Stichinzision durchtrennt. Besser ist es, ein Sehnenstück zu resezieren.
Alternative
Nach lange bestehendem Spitzfuß ist die Fehlstellung im oberen Sprunggelenk durch eine Arthrofibrose fixiert. Dann müssen alle am Unterschenkel dorsal verlaufenden Sehnen durchtrennt, das Gelenk offen arthrolysiert und die 0-Grad-Stellung temporär mit einem K-Draht fixiert werden.
Alternativ ist eine Arthrodese im oberen (und unteren) Sprunggelenk möglich.
Nachbehandlung
Die 0-Grad- Stellung im Sprunggelenk sollte postoperativ für 2 Wochen mit einer Schiene gesichert werden.
Nach der Chopart-Amputation mit Achillessehnendurchtrennung kann der Stumpf schuhtechnisch mit hohem Schaft versorgt werden. Die Patienten schätzen es, wenn sie einen Schuh erhalten, der mit einer Sohlenversteifung und mit einem Platzhalter für Vor- und Mittelfuß ausgestattet ist.
Wurde die Achillessehne belassen, kann der Versuch mit einem Botta-Rahmen unternommen werden (Baumgartner 2011). Nach unserer Erfahrung ist das Risiko für ein Ulkus aber dennoch hoch.
Pirogoff Amputation
Es handelt sich bei der Pirogoffamputation um die Fußamputation unter Belassen des Calcaneus mit anschließender tibiocalcanearer Fusion. Der Stumpf ist „endbelastbar“ mit dem Vorteil gegenüber der Exartikulation im Sprunggelenk (Syme), dass die Beinlänge nur um ca. 2-3 cm verkürzt wird, was das Gehen für kurze Strecke ohne schuhtechnische Hilfe möglich macht. Der Nachteil liegt in Heilungszeit von 6- 8 Wochen bis zur knöchernen Durchbauung und dem Risiko einer Pseudarthrosenentwicklung.
Die Pirogoff-Amputation ist für die Patienten funktionell deutlich günstiger als eine Syme-Amputation.
Alternative:
Bei septischer Destruktion des Talus ist es häufig möglich, den Talus zu entfernen und nach Beruhigung der Infektion eine tibiocalcaneare Fusion vorzunehmen.
Indikationen
Entzündliche Destruktion des Fußes bei Erhalt des Calcaneus und der Ferse.
- Kontraindikationen
- Minderperfusion im Rückfuß. Bei einer PAVK ist die Pirogoffamputation selten möglich, weil die sichere Durchgängigkeit des calcanearen Astes der A. tibialis posterior unbedingt notwendig ist.
- Unfähigkeit der Patienten, den Stumpf 8 Wochen zu entlasten.
Operationstechnik
Zunächst erfolgt ein querer Hautschnitt dorsal des Chopart-Gelenks. Medial biegt der Schnitt in Höhe des „Äquators“ nach distal unter Bildung eines großen plantaren Lappens um (Abb. 47). Dessen Spitze liegt etwa am proximalen Drittelpunkt der Metatarsalia. Es erfolgt die Exartikulation im Chopartgelenk.
Bei der Präparation ist es wichtig, die A. plantaris bis zum distalen Wundrand zu erhalten, um einen Durchblutungsausfall an den Weichteilen zu vermeiden. Die Weichteile müssen deshalb unmittelbar am Periost abpräpariert werden.
Zur Entfernung des Talus verlängert man lateral die Inzision bis hinter den Außenknöchel. Nach Osteotomie der Außenknöchelspitze lässt sich der Talus einfach heraus präparieren. Der Innenknöchel wird zusammen mit der tibialen Gelenkfläche reseziert.
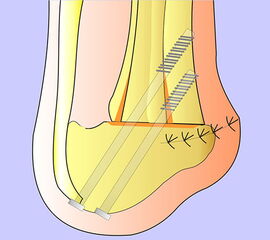
Der kraniale Calcaneus wird so mit der oszillierenden Säge reseziert, dass bei der Fusion mit der Tibia die physiologische Inklination von 30° wieder hergestellt wird (Abb. 48). Wird der Calcaneus zu steil eingestellt, kann das zu erhöhter Druckbelastung am Tuber calcanei und damit zur Ulzeration führen. Eine flache Einstellung des Talus wird von manchen Operateuren bevorzugt. Dies ist technisch vielleicht etwas einfacher, führt jedoch zu einer stärkeren Verkürzung. Varus- und Valgusfehlstellungen müssen vermieden werden.
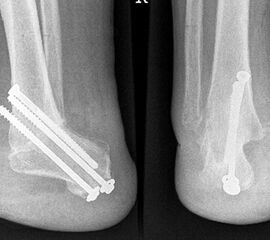
Zur Osteosynthese bevorzugen wir 2-3 kanülierte Großfragmentschrauben (Abb. 49). Postoperativ ist die Extremität für 8 Wochen zu entlasten, wobei zur Sicherheit eine Entlastungsorthese verordnet werden kann. Bei schwachen oder unzuverlässigen Patienten empfiehlt es sich, für 8 Wochen einen Ring-Fixateur anzulegen.
Nachbehandlung
Maßschuh mit ca. 20 cm Schaft und Längenausgleich und Abrollhilfe. In Einzelfällen kann eine orthopädietechnische Versorgung sinnvoll sein. Pirogoff-Stümpfe können mit einem Weichwand-Innenschaft unter Einbeziehung des Unterschenkels versorgt werden. Durch die amputationsbedingte Verkürzung des Beins beim Pirogoff-Stumpf von 3-4 cm ist der Einsatz von speziellen Prothesenfüßen möglich.
Kalkaneusteilamputationen, Kalkaneusresektion
Indikationen
- Weichteildefekte, die weder konservativ noch plastisch-chirurgisch zu decken sind,
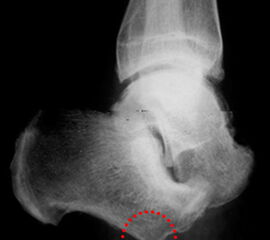
- Lokale Osteomyelitiden mit Knochennekrose und Weichteilbeteiligung (Abb. 50).
- Kontraindikationen
- Bei einer fortgeschrittener PAVK ist eine Calcaneus-Resektion selten ausreichend. Falls nicht eine höhere Amputation indiziert ist, ist meist eine Revaskularisation zusätzlich erforderlich (Abb. 51).
Das Ausmaß der Knochenresektion ergibt sich aus der Defektgröße bzw. aus der Ausdehnung der Osteomyelitis 3 (Abb. 52). Eine totale Kalkanektomie ist problematisch, weil danach die Leitungsbahnen unmittelbar dem Körpergewicht ausgesetzt sind.
Operationstechnik:
In der Regel wird von lateral in der Höhe der vorgesehenen Osteotomie eingegangen (Abb. 53, 54). Ein Zugang von dorsal nach plantar ist möglich. Darüber kann das infektionsauslösende Ulkus existiert werden. Nach Darstellung des Tuber calcanei wird die Osteotomie so angelegt, dass alle osteomyelitisch veränderten Knochenanteile entfernt werden können. Sofern es vertretbar ist, wird der Ansatz der Achillessehne erhalten (Abb. 55).
Die Operationswunde bleibt bis Einsetzen einer sauberen Gratulation offen. Anschließend erfolgt die Sekundärnaht. Das infektauslösende Fersenulkus heilt meist spontan, wenn es nicht bereits beim Primäreingriff exzidiert wurde (Abb. 56).
Nachbehandlung
Nach Wundheilung erfolgt die Versorgung durch eine maßgefertigte Einlegesohle (Abb. 57).
Exartikulation im Sprunggelenk (Symeamputation)
So weit bekannt, wird die Symeamputation in Europa im Gegensatz zu den USA relativ selten vorgenommen. Sie hat im Vergleich zur Unterschenkelamputation folgende Vorteile:
- Das Stumpfende ist wegen der breiten Knochenfläche und der erhaltenen Sohlenhaut endbelastbar, so dass der Amputierte in der Wohnung ohne Prothese einige Schritte gehen kann.
- Der erhaltene Unterschenkel verbessert die Gangökonomie, verglichen zur Unterschenkelamputation.
- Die Prothesenversorgung ist technisch weniger aufwändig und leichter als bei einer Unterschenkelamputation.
Alternative
Wenn es von der Grunderkrankung und dem Lokalbefund her vertretbar ist, sollte der Pirogoff-Amputation der Vorzug gegeben werden, weil die Patienten damit besser gehen können.
Allgemein
Die operationstechnischen Anforderungen für die Syme-Amputation sollten nicht unterschätzt werden. Die Symeamputation ist bei einer PAVK normalerweise nicht indiziert; wenn allerdings die A. tib. post. mit den calcanearen Ästen durchgängig ist, kann sie in Ausnahmefällen vorgenommen werden. Ist die A. tibialis posterior verschlossen, die A. tibialis anterior aber intakt, kann eine „umgekehrte Syme-Amputation“ erwogen werden. Dabei wird ein ventraler Lappen gebildet, der nach dorsal umgeschlagen wird.
Technik
Es erfolgt eine Umschneidung des Fußes distal des Sprunggelenks. Die Schnittführung erfolgt etwas proximal von der für die Pirogoff Amputation. Für die spätere Belastung ist es günstig, wenn Anteile der Fußsohlenhaut unter den Tibiastumpf positioniert werden können. Es werden der dorsale und der plantare Lappen gebildet. Die Spitze des plantaren Lappens reicht ca. bis zum Tarso-metatarsal-Gelenk. Zur besseren Darstellung von Talus und Calcaneus kann die Inzision lateral bis hinter den Außeninnenknöchel verlängert werden.
Der Talus, der Calcaneus sowie Außen- und Innenknöchel werden epiperiostal präpariert, um zuverlässig die A. tibialis posterior zu erhalten. Danach werden die tibiale Gelenkfläche und in dieser Ebene die Malleolen mit der oszillierenden Säge abgetragen (Abb. 60).
Werden Gelenkknorpel und Teile der Synovia belassen, bildet sich eine Art Bursa, durch welche der Weichteilstumpf mit dem Fersenpolster hochgradig beweglich ist. Das führt einerseits zu Gangunsicherheit. Andererseits kann das Weichteilpolster so weit verrutschen, dass im Bereich eines Knöchels normale Haut (also keine Fußsohle) belastet wird und dort ein Ulkus entsteht (Abb. 59, 60).
Zur Vermeidung der Dislokation des Weichteilpolsters wird in der Literatur die Fixierung der Achillessehne an die Tibia empfohlen (Bevilaqua 2013) 45. Nach unserer Erfahrung reicht die Durchtrennung der Sehne aus. Noch besser ist die Resektion von 2 cm Sehnengewebe, um eine Wiedervereinigung der Sehnenstümpfe zu verhindern. Die Resektion der Gelenkfläche begünstigt das Verwachsen des Knochens mit dem Subkutangewebe und unterstützt damit die Fixierung der Weichteile.
Der Wundverschluss erfolgt nach Einlegen einer Drainage. Bisweilen verbleiben medial und lateral oft Hautüberstände. Diese verschwinden durch die Weichteilschrumpfung spontan, solange sie nicht größer als 1 cm sind. Größere Überstände sollten exzidiert werden.
Nachbehandlung
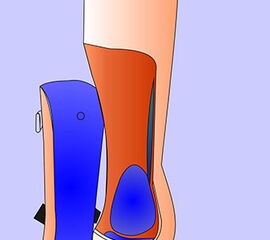
Postoperativ wird ein gut sitzender Kompressionsverband angelegt, um eine Nachblutung zu verhindern. Um das Verwachsen der Tibiaresektionsfläche mit dem Fersenpolster zu begünstigen, wird ein Hartverband oder eine thermoplastische Schiene angelegt. Die Drainage wird nach Sistieren der Sekretion entfernt. Zur Konfigurierung des Stumpfes wird die elastische Bandagierung fortgeführt, die nach Eintreten von trockenen Wundverhältnissen durch einen Silikonliner ersetzt wird. Sobald stabile Wundverhältnisse vorhanden sind, wird eine Prothese angepasst (Abb. 61).
Postoperative Probleme
Bei störender Hypermobilität des Fersenpolsters werden die Achillessehnendurchtrennung und die Resektion der Tibiagelenkfläche gegebenenfalls nachgeholt. Bei der Prothesenversorgung ist darauf zu achten, dass der Stumpf gut gefasst ist, um Scherbewegungen zu vermeiden.
Transtibiale Amputation (Unterschenkelamputation)
Heute gilt die transtibiale Amputation im Bereich des proximalen Drittelpunktes für viele Operateure als Standard-Maßnahme in der Amputationschirurgie. Im Vergleich zu den Zeiten der routinemäßigen Oberschenkelamputation ist das als Fortschritt anzusehen. Dennoch ist in vielen Fällen eine weiter distal gelegene Amputation möglich und für den Patienten von Vorteil. Die Probleme bei der Unterschenkelamputation bezüglich Indikation, Operationstechnik und Nachbehandlung können sich komplex darstellen.
Indikationen
- Nicht revaskularisierbare, fortgeschrittene Durchblutungsminderung bei PAVK. Diese Indikation sowie die Höhe der Amputation sind mit einem Gefäßspezialisten abzustimmen.
- Ausgedehnte, eitrige Infektionen (Abb. 62, 63). Bisweilen ist präoperativ ein MRT zu veranlassen, welche das Ausmaß der Infektion und der Einschmelzung dargestellt.
Prinzipien
Zur Frage, an welcher Höhe die Absetzung im Vergleich zur Infektion zu erfolgen hat, ist festzustellen, dass nekrotisierende Infektionen immer entfernt werden müssen. Vitales, gut durchblutetes Gewebe, speziell Muskulatur und Haut, hat die Möglichkeit, eine bakterielle Infektion zu überwinden. Es kann deshalb in Form einer in „offenen Amputation“ belassen werden. Der Fall, der in Abb. 62 und 63 dargestellt ist, wurde entsprechend mit einer offenen Amputation im proximalen Drittelpunkt des Unterschenkels behandelt.
Es können lange Unterschenkelstümpfe erzeugt werden (Abb. 64 und 65), auch wenn einige Autoren diese kritisch sehen. Voraussetzung für einen langen Unterschenkelstumpf ist eine ausreichende Perfusion und die Infektfreiheit vor dem Wundverschluss. Ein langer Stumpf hat zwar das Problem einer geringeren Weichteildeckung im Endbereich. Mit einer korrekten Operationstechnik lässt sich das Knochenende jedoch ausreichend polstern, zumal die Lastübertragung vom Körpergewicht auf die Prothese überwiegend am Tibiakopf erfolgt. Der entscheidende Vorteil eines langen Stumpfes ist, dass die Patienten einen geringeren Energieverbrauch und damit eine höhere Lebensqualität haben 6.
Umgekehrt kann, falls erforderlich, die Unterschenkelamputation nach proximal bis zum Ansatz der Patellarsehne an der Tuberositas tibiae ausgedehnt und das Kniegelenk erhalten werden (Abb. 66 und 67).
Operationstechnik
Bei hinreichender Durchblutung kann in Oberschenkelblutsperre operiert werden, wenn keine Bypassoperationen oder Stents vorliegen. Fuß und distaler Unterschenkel werden in eine Stockinette eingepackt. Ziel ist es, den Stumpf im Hinblick auf die Prothesenversorgung so zu konfigurieren, dass er einem Konus oder einem Zylinder möglichst nahe kommt.
Schnittführung: Wir führen entweder einen abgewinkelten Schnitt unter Bildung eines großen dorsalen und eines kleinen ventralen Lappens durch (Abb. 64, 66). Die Tibia lässt sich dadurch gut mit Muskel bedecken. Auch eine „maulartige“ oder „sagittale“ Schnittführung ist möglich (Abb. 68). Die Strukturen werden Schritt für Schritt senkrecht zur Haut durchtrennt.
Weichteilpräparation: Es empfiehlt sich, frühzeitig die großen Gefäße aufzusuchen und vor der Durchtrennung zu ligieren besonders, wenn ohne Blutsperre gearbeitet wird. Die Nervenstämme werden etwas nach proximal verfolgt, unterbunden und durchtrennt. Die Ligatur verhindert das Aussprossen von Nervenfasern und damit die Bildung von Neuromen sowie das Verwachsen der Nervenfasern mit Sehnen, Faszien oder Narbengewebe. Mit dieser Technik lässt sich das Risiko von Phantomschmerzen weitgehend ausschließen (Baumgartner 1995).
Der M. soleus wird bei einer proximalen Amputation entfernt (Abb. 69). Nach Entfernen des M. soleus wird der dorsale Weichteillappen hoch geklappt und die Faszien der dorsalen und ventralen Muskulatur miteinander vernäht. Bisweilen ist es sinnvoll, die Faszie transossär zu fixieren (Abb. 70). Wird der M. soleus belassen, besteht aufgrund seiner retrograden Gefäßversorgung die Gefahr der Gefäßunterbrechung und damit einer Muskelnekrose. Gleichzeitig geht mit dem Erhalt der großen Muskelmasse nach Verschluss der Weichteile die Ausbildung der unerwünschten „Birnenform“ einher, was für die spätere prothetische Versorgung ungünstig ist (Abb. 71).
Knochenpräparation: Die Tibia wird in der Höhe durchtrennt, die einen spannungsfreien Wundverschluss ermöglicht. Die Tibiavorderkante wird abgeschrägt, um Knochendruck auf die Haut zu vermeiden. Die Fibula wird ca. 1-2 cm proximal der Tibia durchtrennt (Abb. 65 und 67). Bei sehr kurzen Stümpfen wird die Restfibula entfernt, damit sie nicht wegen des Fehlens der Membrana interossea valgisch absteht.
Die Knochenstümpfe werden mit Faszien- und Muskelgewebe abgedeckt (Abb. 70).
In einer tibio-fibularen Synostosierung durch Spongiosaanlage oder Periostverlagerung mit dem Ziel, die distale Knochenfläche zu vergrößern und damit die Endbelastbarkeit zu erhöhen, haben wir keinen Vorteil gesehen (Ertl 1949).
Abschluss: Eine sorgfältige Blutstillung ist notwendig, weil Hämatome lästige Heilungsstörungen nach sich ziehen können.
Nach Einlegen einer Drainage wird der dorsale Lappen hoch geklappt und die Faszien so vernäht (Abb. 72). Die Zuverlässigkeit der Stumpfabdeckung kann durch transossäre Fasziennähte erhöht werden. Bei einer dicken Subkutanschicht werden zusätzliche Subkutannähte angelegt. Die Haut wird mit lockeren Einzelknopfnähten verschlossen. An der medialen und lateralen Wundecke können Hautüberstände („Hundeohren“) verbleiben (Abb. 73), die durch Winkelschnitte beseitigt werden können (Abb. 74-76).
Zu achten ist auf einen gut sitzenden elastischen Kompressionsverband, der bei einer PAVK nur vorsichtig angezogen werden darf. Dieser soll einerseits zur Verhinderung der Nachblutung und andererseits zur Stumpfkonfiguration beitragen (Abb. 77). Die Ruhigstellung in einem Cast begünstigt die Wundheilung.
Nachbehandlung
Die Verbände werden anfangs täglich gewechselt, auch um die Kompression auf dem Stumpf aufrecht zu erhalten. Die Kompressionsverbände beschleunigen die Abschwellung der Weichteile. Außerdem begünstigen sie die Ausbildung eines „prothesenfähigen“ Stumpfes (Abb. 78). Durch Ruhigstellung in einem Hartverband wird die Wundheilung verbessert.
Wenn die Wunden trocken sind, wird ein Silikonliner zur Formierung des Stumpfes angelegt. Es ist darauf zu achten, dass das Knie in Streckung gelagert wird, um die eine Beugekontraktur zu vermeiden.
Es sollte frühzeitig mit dem Orthopädietechniker Kontakt aufgenommen werden, damit entschieden werden kann, wann mit der Prothesenversorgung begonnen wird.
Die Auswahl der Prothese richtet sich nach dem Mobilisationsgrad (Baumgartner 1995).
0 = nicht gehfähig: Es kommt allenfalls eine „kosmetische“ Prothese in Betracht
1 = Innenbereichsgeher: Prothese zum Transfer zum Rollstuhl und für wenige Schritte in der
Wohnung
2= eingeschränkter Außenbereichsgeher: Prothese zum Gehen auf begrenzter Gehstrecke
3= uneingeschränkter Außenbereichsgeher: Prothese für das allgemeine Gehen im Alltag
4 = Sportler: Prothesen mit besonders hohen Ansprüchen.
Komplikationen
- kleine Hämatome werden durch Öffnen der Wunde abgelassen. Wenn größere Hämatome vorliegen, werden diese unter sterilen Kautelen im Operationssaal ausgeräumt.
- Hohe Spannung auf der Naht: Die Fäden werden eröffnet. Es erfolgt der sekundäre Verschluss u. U. durch plastisch-chirurgische Maßnahmen oder durch Nachkürzen des Knochens.
- Infektion: Eröffnen der Wunde und Debridement im Op. Evtl. Unterdruckverband, nachdem der wesentliche Teil der Infektion beherrscht ist.
- Durchblutungsstörung z.B. durch neuen Gefäßverschluss. Es muss eine neue angiologische Klärung erfolgen. Mögliche therapeutische Konsequenzen sind Gefäßintervention oder Nachamputation.
- In der Operationsnarbe können Fisteln entstehen. Wenn diese konservativ nicht zur Heilung zu bringen sind, werden sie operativ revidiert. Dabei werden nekrotische Gewebeanteile oder Fadenreste entfernt. Es erfolgt der schichtweise Wundverschluss, wobei insbesondere die ehemalige Infektionshöhle mit vitalem Gewebe aufgefüllt und verschlossen wird (Abb. 79, 80). Die temporäre Einlage einer Antibiotikakette kann sinnvoll sein.
- Wundheilungsstörungen aufgrund von infizierten Nekrosen erfordern ein konsequentes, eventuell wiederholtes Debridement. Es ist zu entscheiden, ob ein unmittelbarer oder verzögerter Hautverschluss erfolgen kann oder ob die Sekundärheilung vorzuziehen ist (Abb. 81-83.).
- Wundheilungsstörungen können sich ergeben, wenn die Vereinigung von ventraler und dorsaler Faszie nicht eingetreten ist oder wenn die Haut in zu großer Spannung verschlossen wurde, meist bei zu wenig reseziertem Knochen (Abb. 84, 85). In beiden Fällen ist eine Revision mit Nachresektion von Knochen, Entfernung überflüssiger Muskulatur (sowie Nekrosen) und erneuter Fasziennaht erforderlich.
Knieexartikulation
Die Knieexartikulation muss immer erwogen werden, wenn die Unterschenkelamputation nicht ausreichend ist. Sie ist, sofern sie vom Krankheitsgeschehen möglich ist, wesentlich günstiger als die transfemorale Amputation. Von der operativen Technik ist sie einfacher durchzuführen und bedingt einen geringen Blutverlust. Die postoperative Erholung erfolgt schneller bei weniger Komplikationen. Außerdem bietet sie einen endbelastbaren Stumpf, der durch die Oberschenkelmuskulatur gut positioniert werden kann. Der Energieverbrauch ist deutlich geringer als bei der Oberschenkelamputation. Nachteilig ist nur der Umstand, dass bei der Prothesenversorgung die Gelenklinie um einige Zentimeter nach distal verlagert wird und bei gebeugtem Kniegelenk das Prothesenknie um einige cm übersteht.
Operationstechnik
Bei der Operation wird ein großer dorsaler oder auch ein ventraler Lappen ohne Muskeln präpariert (Baumgartner 2002) (Abb. 86). Die Menisci und die Patella können entfernt oder belassen werden. Teile der Femurkondyle können reseziert werden. Der Wundverschluss erfolgt durch Faszien-, Sukutan- und Hautnähte.
Unter http://www.youtube.com/watch?v=sCc8t_Mx92Q kann die korrekte Op-Technik verfolgt werden. (Die Frage, ob im dargestellten Fall auch eine weiter distal gelegene Amputation ausreichend gewesen wäre, muss offen bleiben.)
Nachbehandlung
Die Nachbehandlung besteht anfänglich in den üblichen Kompressionsverbänden mit Hartverband und später in dem Silikonliner sowie abschließender Prothesenversorgung (Abb. 87).
Transfemorale Amputation (Oberschenkelamputation)
Indikation
- Durchblutungsausfälle
- ausgedehnte Infektionen,
- selten Tumore und schwere Traumen, die mit einer Knieexartikulation nicht zu versorgen sind.
Operationstechnik
Grundsätzlich sollte so viel wie möglich von dem Oberschenkel bzw. dem Femurknochen erhalten bleiben; denn je kürzer der Knochen, umso mehr kommt die abduzierende Wirkung der pelvitrochanteren Muskeln zur Geltung. Außerdem ermöglicht ein langer Stumpf eine bessere Führung der Prothese.
Die Schnittführung kann so gewählt werden, dass ein medialer und ein lateraler, aber auch ein ventraler und ein dorsaler Lappen gebildet werden (Abb. 88). Von der am besten
erhaltenen Muskulatur werden Lappen gebildet, die das Resektionsende den Knochenstumpf ausreichend überragen.
Nach Durchtrennung des Knochens werden die antagonisierenden Muskeln über die Faszien miteinander vernäht, sodass der Knochenstumpf sicher abgedeckt ist. Wenn die Fixierung der Muskulatur auf diese Weise nicht ausreichend sicher erscheint, sollte eine transossäre Fixation über ein Bohrloch vorgenommen werden (Abb. 89).
In der Regel werden zwei große Drainagen eingelegt. Es folgen Subkutan- und Hautnähte (Abb. 90).
Nachbehandlung
Die Stumpfkonditionierung erfolgt durch Verbandwechsel und elastische Binden, Hartverband sowie durch Silikonliner, wie bei der transtibialen Amputation beschrieben. Nach Wundheilung beginnt die Planung der Prothesenversorgung.
Schlussbemerkungen
Amputationen im Zusammenhang mit dem diabetischen Fußsyndrom (DFS) bringen in vielerlei Hinsicht erhebliche Probleme mit sich. Das mit Abstand größte Problem ist die Tatsache, dass weiterhin erheblich zu viel amputiert wird. So ist es bislang trotz verschiedener internationaler Aktivitäten nicht gelungen, im Bereich des neuropathischen Fußes und der Infektionen anerkannte und nachvollziehbare Indikationen zu erarbeiten. Die bestehenden Klassifikationen zu Infektionen im Fußbereich wie die IDSA und die PEDIS Klassifikation geben keine zuverlässigen Anhaltspunkte zur Amputationsindikation. Entsprechend gibt es keine Liste von Alternativen bzw. Salvage-Maßnahmen, um Fuß erhaltend vorzugehen.
Die Herausforderung für den behandelnden Arzt ist die präzise Indikationsstellung sowie die Einbeziehung von Therapiealternativen in die Behandlungsstrategie. Wichtig ist es, unter Kenntnis auch selten durchgeführter Techniken die richtige Amputationshöhe festzulegen, um ein für den Patienten optimales Resultat zu erreichen. Eine Amputation ist ein anspruchsvoller Eingriff, bei welchem Fehler erhebliche Auswirkungen haben. Die Nachbehandlung erfolgt nicht nur durch schuh- und orthopädietechnische Hilfsmittel, sondern ganz wesentlich auch durch Physiotherapie. Sehr wichtig wäre es, für Patienten mit größeren Amputationen und eingeschränktem Allgemeinzustand stationäre Rehabilitationseinrichtungen zur Verfügung zu stellen. Bei entsprechendem Vorgehen lässt sich die Lebensqualität der Patienten wesentlich verbessern.
Weitere Literatur
- Barouk LS. Forefoot Reconstruction. Springer Verlag Paris, Berlin 2005
- Baumgartner R. Amputationen im Bereich des Fußes S. 358 – 390. In: Becken und untere Extremität. Thieme Verlag, Stuttgart, 1995.
- Baumgartner R, Botta P. Amputation und Prothesenversorgung der unteren Extremität. Enke Verlag, Stuttgart, 1995.
- Baumgartner R, Greitemann B. Grundkurs Technische Orthopädie. Thieme Verlag, Stuttgart - New York, 2002.
- Baumgartner R, Möller M, Schäfer M. Amputation und Prothesenversorgung. In: Baumgartner R., Möller M., Stinus H. Orthopädieschuhtechnik. Maurer Verlag, Geislingen, 2011.
- Bevilacqua NJ, Rogers LC, Armstrong DG. Pedal Amputation in Diabetes. In: Saxena A (ed). Special Procedures in Foot and Ankle Surgery. Springer Verlag, London, 2013.
- Bowker JH. Minor and Major Lower-Limb Amputation and Disarticulation in Patients with Diabetes mellitus (pp: 403-428). In: Bowker JH, Pfeifer MA (eds). The Diabetic Foot. Mosby Elsevier, Philadelphia, 2008.
- Brodsky JW. Amputation of the Foot and Ankle. In: Coughlin MJ et al. (ed). Surgery of the Foot and Ankle. Mosby Elsevier, Philadelphia, 2007.
- Burgess EM, Romano RL, Zettl JH. Prosthetic Research Study. The management of lower extremity amputations: surgery, immediate postsurgical prosthetic fitting, patient care. Washington, DC: US Government Printing Office, 1969.
- Eckhardt A, Lobmann R. Der diabetische Fuß. Springer Verlag, Heidelberg, 2005.
- Ertl J. Über Amputationsstümpfe. Chirurg. 20:218-24, 1949.
- Hochlenert D, Engels G, Altenhofen L: Integrierte Versorgung: Ergebnisse des Netzwerks Diabetischer Fuss Köln und Umgebung. Dtsch Ärztebl 103:A1680-1683; 2006.
- Hochlenert D, Engels G, Morbach S: Das diabetische Fußsyndrom - Über die Entität zur Therapie, Springer Verlag, Berlin Heidelberg, 2014.
- Koester R. Amputationstechniken. In: Köck FX, Koester B (ed). Diabetische Fußsyndrom. Praxiswissen Halte- und Bewegungsorgane. Thieme Verlag, Stuttgart New York, 2007.
- Rhim B, Baravarian B, Zgonis T. A stepwise approach to Diabetic Foot and Ankle Amputations (p. 392-410). In: Zgonis T (ed). Surgical Reconstruction of the Diabetic Foot and Ankle. Wolters Kluwer Lippincott Williams & Wilkins, Philadelphia, 2009.
- Morbach S, Müller E, Reike H, Risse A, Rümenapf G, Spraul M. AWMF Leitlinie Diabetisches Fußsyndrom. Ind: Scherbaum WA, Haak T (eds). Deutsche Diabetes
Gesellschaft. Deutsche Gesellschaft für Gefäßchirurgie, 2008.